Что называется углеродным скелетом
Углеродный скелет
Углеродный скелет молекулы — последовательность химически связанных атомов углерода, составляющая основу молекулы. Кроме атомов углерода в состав скелета могут входить и другие атомы, например, кислород, сера, азот, если они связаны, по меньшей мере, с двумя атомами углерода. Некоторые атомы углерода в углеродном скелете могут быть соединены с тремя или даже четырьмя другими атомами углерода, такой углеродный скелет называют разветвлённым.
Например, в диметиловом эфире СН3-О-СН3 атом кислорода включен в скелет молекулы, а в этаноле — CH3CH2-OH — нет. Молекулы, в скелет которых, кроме атомов углерода, входят атомы других элементов, называются гетероатомными (лат. getero — «разный»).
Типы углеродных скелетов
Углеродные скелеты разделяют на следующие типы:
В гетероциклическом скелете в углеродный цикл включается одни или несколько атомов, отличных от углерода. Исторически сложилась традиция не рассматривать такие гетероатомы как функциональные группы, а считать их частью углеродного скелета. Примером гетероциклического соединения может служить печально известный никотин: 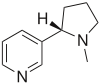
В самих углеродных скелетах нужно классифицировать отдельные атомы углерода по числу химически связанных с ними атомов углерода. Если данный атом углерода связан с одним атомом углерода, то его называют первичным, с двумя — вторичным, тремя — третичным и четырьмя — четвертичным.
Поскольку атомы углерода могут образовывать между собой не только одинарные, но и кратные (двойные и тройные) связи, то соединения, содержащие только одинарные связи углерод—углерод, называют насыщенными, соединения с кратными углерод-углеродными связями называют ненасыщенными. Соединения, в которых атомы углерода связаны только с атомами водорода, называют углеводородами.
Ссылки
Полезное
Смотреть что такое «Углеродный скелет» в других словарях:
Никотин — C10H14N2 представляет алкалоид табака, в листьях которого он находится в количестве 0,6 8,0%. В плохих сортах табака его больше, чем в хороших. Кроме того, сочные и мясистые листья имеют его также больше, чем тонкие. Н. жидок, гонится без… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Макролиды — обширная группа антибиотиков (См. Антибиотики), в структуру которых входит многочленный лактонный цикл. Все известные М. выделены из почвенных грибов рода Streptomyces и по строению и физиологическому действию разделяются на две подгруппы … Большая советская энциклопедия
Терпены и их производные — класс соединений, важных в практическом отношении и весьма интересных в теоретическом; большею частью вырабатываются и выделяются растениями в виде так наз. эфирных масел (см.), но известно также много искусственно получаемых представителей этого … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Хинин (хим.) — С20Н24О2N2.3Н2О алкалоид, встречающийся совместно с цинхонином и многочисленными другими алкалоидами в виде хинодубильных и хинокислых солей, особенно в корах цинхон (Cinchona Calysaya, С. offocinalis, С. succirubra, С. Ledgeriana и их… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ОБМЕН ВЕЩЕСТВ — (метаболизм), совокупность хим. процессов, обеспечивающих жизнедеятельность организма. Хим. превращ. в организме осуществляются в двух противоположных направлениях синтез сложных соед. из более простых (а н а б о л и з м, или а с с и м и л я ц и… … Химическая энциклопедия
триозы — простейшие углеводы (углеродный скелет состоит из 3 атомов) глицериновый альдегид и диоксиацетон. Образуются в растениях в процессе фотосинтеза, важные промежуточные продукты обмена веществ. * * * ТРИОЗЫ ТРИОЗЫ, простейшие углеводы (углеродный… … Энциклопедический словарь
Терпеноиды — Терпеноиды кислородсодержащие органические соединения (как правило, природного происхождения), углеродный скелет которых образован из изопреновых звеньев. Терпеноиды являются производными терпенов, в некоторых случаях их углеродный… … Википедия
Сапонины — Сапонины безазотистые[1] гликозиды растительного происхождения с поверхностно активными свойствами. Растворы сапонинов при взбалтывании образуют густую стойкую пену. Название происходит от латинского sapo (род. падеж saponis) мыло[2] … Википедия
Химическое строение — Настоящая статья имеет задачей изложение истории возникновения теории X. строения органических соединений и ее связи с предыдущими теориями. В значительной мере это уже выяснено в статьях Замещение, Унитарная система, Химических типов теория и… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Химия природных соединений — (ХПС) раздел органической химии, изучающий химические соединения, входящие в состав живых организмов, природные пути их превращений и методы искусственного получения. Как наука, химия природных соединений возникла одновременно с… … Википедия
Что называется углеродным скелетом
Для классификации органических веществ по типам и построения их названий в молекуле органического соединения принято выделять углеродный скелет и функциональные группы.
1) ациклические (не содержащие циклов) – соединения с открытой (незамкнутой) цепью углеродных атомов (прямой или разветвленной):
Такие соединения называются также алифатическими или соединениями жирного ряда. Они могут быть предельными, или насыщенными (парафины, или алканы), и непредельными, или ненасыщенными: соединения ряда этилена (олефины или алкены) и ацетилена (алкины):
2) циклические соединения – соединения, в которых углеродные атомы образуют циклы.
Циклические соединения разделяются на 2 подтипа:
а) карбоциклические – циклические соединения, образованные только углеродными атомами. Они подразделяются на алициклические (нафтены) и ароматические соединения. Алициклические соединения могут быть насыщенными (циклоалканы) и ненасыщенными (циклоалкены):

б) гетероциклические соединения – циклы, в состав которых, кроме атомов углерода, входят и другие атомы – гетероатомы (N, S, O и другие):
В самих углеродных скелетах отдельные атомы углерода классифицируют по числу связанных с ними атомов углерода:
(функциональные группы) При замещении одного или нескольких атомов водорода в углеводородах на другие атомы или группы атомов образуются различные производные углеводородов – классы органических соединений. Такие группы называются функциональными.
1. Что называется углеродным скелетом?
1. Что называется углеродным скелетом?
Какие виды скелетов Вам известны?
Приведите примеры в виде структурных формул 2.
Какие виды органических соединений Вы знаете в зависимости от строения углеродного скелета?
Углеродный скелет молекулы — последовательность химически связанных атомов углерода, составляющая основу молекулы.
Кроме атомов углерода в состав скелета могут входить и другие атомы, например, кислород, сера, азот, если они связаны, по меньшей мере, с двумя атомами углерода.
Некоторые атомы углерода в углеродном скелете могут быть соединены с тремя или даже четырьмя другими атомами углерода, такой углеродный скелет называют разветвлённым.
Глеродные скелеты разделяют на следующие типы :
ациклические (не содержащие циклов), например, бутан.
Циклические, например, бензол.
Гетероциклические(В гетероциклическом скелете в углеродный цикл включается одни или несколько атомов, отличных от углерода).
Напишите структурные формулы структурных изомеров :а)углеродного скелетаб)положения двойной связив)пространственного строенияг)межклассовых алкенов состава С6Н12 и назовите их по систематической номен?
Напишите структурные формулы структурных изомеров :
б)положения двойной связи
г)межклассовых алкенов состава С6Н12 и назовите их по систематической номенклатуре.
2. Исходя из молекулярной формулы пропана 8 запишите : углеродный скелет этого вещества.
Молекулы какого вещества могут иметь разветвленный углеродный скелет?
Молекулы какого вещества могут иметь разветвленный углеродный скелет.
Помогите определить у какому классу органических соединений относятся вещества и назовите их по систематической номенклатуре?
Помогите определить у какому классу органических соединений относятся вещества и назовите их по систематической номенклатуре.
Приведите структурные формулы двух веществ, имеющих молекулярную формулу С4H8?
Приведите структурные формулы двух веществ, имеющих молекулярную формулу С4H8.
Назовите эти вещества по систематической номенклатуре.
К каким классам органических соединений относятся эти вещества?
К каким классам органических соединений относятся эти вещества?
Назовите по международной номенклатуре следующие соединения :
Напишите структурные формулы изомеров алкенов состава С5Н10 1) углеродного скелета «2)положение двойной связи 3)межклассовых назовите их по систематической номенклатуре?
Напишите структурные формулы изомеров алкенов состава С5Н10 1) углеродного скелета «2)положение двойной связи 3)межклассовых назовите их по систематической номенклатуре.
Назвать каждое вещество по систематической номенклатуре?
Назвать каждое вещество по систематической номенклатуре.
Для вещества под а)написать сокращенные структурные формаулы двух изомеров углеродной цепи.
Для вещества под б)написать сокращенную структурную формулу одного гомолога с более длинной углеродной цепью.
Назвать каждое вещество.
Дать определение номенклатура и написать какие виды номенклатуры свойственны органическим веществам?
Дать определение номенклатура и написать какие виды номенклатуры свойственны органическим веществам.
1s²2s²2p63s²3p³, только шесть тоже маленькая.
W(массовая доля) = m(растворенного вещества / m(раствора) Масса раствора равна 90г + 180г = 270г w = 90г / 270г = 0. 333. (33. 3%).
HCL + CA→ HCL + NAOH→ HCL + DS→.
2HCl + Ca➡CaCl2 + H2 HCl + NaOH➡NaCl + H2O.
Что называется углеродным скелетом
Углерод – базовый элемент нашей планеты. Он занимает менее 0.1% от массы Земли, но это один из самых «активных» элементов планеты. Атомы углерода постоянно мигрируют из одной части биосферы Земли в другую.
Эта статья была опубликована в журнале OYLA №5(21). Оформить подписку на печатную и онлайн-версию можно здесь.
Как видите, в природе углерод встречается практически повсюду. Он является незаменимым участником всех химических процессов, происходящих c живыми организмами. Но и в повседневной жизни человечество не может отказаться от углерода. Ежедневно мы потребляем разнообразные материалы и вещества, содержащие углерод. Это нефтепродукты, горючее, топливо, полимерные материалы (каучуки, пластмасса, волокна, плёнки, лаки, клеи, одежда), а также красители, средства защиты растений, лекарственные препараты, вкусовые и парфюмерные добавки и т.д. Получается, что человеку без углерода – никуда!
Углерод — особый элемент, потому что способен образовывать огромное многообразие органических соединений. А собственно, почему именно углерод оказался тем «счастливчиком», которому природа, а затем и человек, предоставили «эксклюзивное» право быть основой для разнообразных по своим свойствам веществ? И ещё: почему именно водород стал основным «напарником» углерода в органических соединениях? Чтобы ответить на эти вопросы, нужно рассмотреть строение атомов углерода и водорода.
Строение атома углерода можно представить в виде так называемой планетарной модели, которую предложил английский физик-химик Эрнест Резерфорд, получивший за это Нобелевскую премию. Атом представляет собой мини-солнечную систему, в центре которой находится «солнце» — положительно заряженное ядро, а вокруг вращаются планеты солнечной системы — электроны. Следует отметить, что планетарная модель атома углерода — это упрощённая модель. В действительности же, электроны в атоме углерода двигаются по несколько сложной траектории. Но мы используем планетарную модель, так как она наглядна и достаточна, чтобы объяснить, как взаимодействуют между собой атомы и как они связываются друг с другом.
Эрнест Резерфорд
Основатель науки об атомном ядре. Свои главные открытия он сделал уже после получения Нобелевской премии. В 1911 году ему удался эксперимент, который позволил заглянуть вглубь атома и получить представление о его строении.
Но сначала рассмотрим группу элементов, атомы которых слабо взаимодействуют с атомами других элементов. Это благородные газы, такие как неон (Ne), аргон (Ar) и ксенон (Xe). В чём причина такого свойства? Всё дело в электронах!
У благородных газов (кроме гелия) во внешней оболочке ровно 8 электронов. Именно такое количество электронов делает электронную оболочку атома стабильной. Именно из-за этой «стабильности» атомы благородных газов не нуждаются в других электронах, у них всего достаточно. Углерод тоже «мечтает» стать благородным, поэтому он стремится заполнить свою внешнюю оболочку до 8 электронов. Ему необходимо ещё 4 электрона, чтобы он наконец стал благородным и успокоился. Водород тоже «мечтает» стать благородным. Но водороду легче, чем углероду: ему достаточно «добыть» себе один электрон, и он станет похож на благородный газ гелий (He) (у гелия, как и у водорода одна оболочка, но с двумя электронами).
Получается, что и атомам углерода, и атомам водорода нужны электроны. Откуда же их взять? Собравшись вместе, атомы углерода и водорода начинают делиться своими электронами друг с другом. Нет, не думайте, что они начинают отдавать или принимать электроны. Ведь в таком случае, кто-то останется «обиженным», то есть без электронов. Атомы углерода и водорода поступают мудрее. Они подходят друг к другу и «говорят»: давай объединимся и сделаем наши электроны общими. Поскольку атому водорода нужен только один электрон, ему достаточно «договориться» с одним атомом углерода. А вот атому углерода придётся «потрудиться» и договориться с четырьмя.
Как видите, у углерода 8 электронов, у атомов водорода — по 2. Все «довольны» и все могут делать вид, что они стали благородными. Электронная формула метана записывается таким образом:
В структурной формуле метана общая пара электронов заменяется чёрточкой.
Вариант 2. Атом углерода может «договориться» с одним атомом углерода и тремя атомами водорода. Тогда второму атому углерода надо будет присоединить к себе ещё три атома водорода. В этом случае получится газ этан — С2Н6.
Вариант 2.2. Иногда между атомами углерода возникает не одинарная, а двойная или тройная связь, то есть у них не одна общая пара электронов, а две или три. Тогда им для «полного счастья» нужно меньше атомов водорода. Например, этилен (С2Н4) и ацетилен (С2Н2).
Вариант 3. Если к двум атомам углерода захочет присоединиться третий атом углерода — добро пожаловать! Получился газ пропан — С3Н8.
Каждый раз, присоединяя по одному атому углерода, мы будем получать новое вещество: бутан, пентан, гексан, гептан, октан. И так можно до бесконечности. Например, в основе молекулы ДНК лежит несколько сотен миллионов атомов углерода.
Вы увидели, что атомы углерода очень «коммуникабельны»: они прекрасно могут «договариваться» между собой и при этом образовывать самые разнообразные не только по длине, но и форме цепи. Эти цепи называются углеродными скелетами. Они могут быть
Углеродный скелет — это последовательность химически связанных атомов углерода, составляющая основу молекулы.
Вариант 4. Рассмотрим вещество гексан — С6Н14. Он имеет линейный углеродный скелет.
Если же атомы углерода «захотят», то они могут замкнуть кольцо, тогда получится газ циклогексан — C 6H12 или газ бензол — C6H6, молекулы которых имеют циклический углеродный скелет.
Но на этом изобретательность атомов углерода не заканчивается. Они могут ещё образовывать разветвлённые углеродные скелеты.
Вариант 5. Есть газ бутан. Его молекула состоит из 4 атомов углерода и 10 атомов водорода — C4H10.
А ещё есть газ изобутан. Его молекула также состоит из 4 атомов углерода и 10 атомов водорода — C 4H10. В то же время это два разных газа: изобутан имеет более низкие температуры плавления и кипения, чем бутан. В чём же подвох? А подвоха никакого нет, есть разные углеродные скелеты.
Бутан имеет линейный углеродный скелет, изобутан — разветвлённый. То есть, бутан и изобутан — изомеры.
Разница в строении может сказываться не только на химических свойствах веществ, но и на физических, таких как запах. Например, возьмём довольно простое органическое соединение — ванилин и его изомер — изованилин. Ванилин — одно из наиболее известных душистых веществ, его приятный запах знаком каждому с детства. А изованилин при нормальных условиях почти не пахнет, если же его нагреть, распространится малоприятный запах, похожий на запах гуаши. Ароматы разительно отличаются, а разницы в составе нет — C 8H8O3
Таким образом, благодаря особенностям атома углерода, его соединения с водородом и другими элементами весьма многочисленны и разнообразны, а органическая химия — одна из наиболее развитых фундаментальных наук. Она является основой многих дисциплин, таких как:
Что называется углеродным скелетом
Основные понятия органической химии
Органическая химия – это область химии, изучающая соединения углерода. Углерод выделяется среди всех элементов тем, что его атомы могут связываться друг с другом в длинные цепи или циклы. Именно это свойство позволяет углероду образовывать миллионы соединений, изучением которых занимается органическая химия.
Теория химического строения А. М. Бутлерова.
Современная теория строения молекул объясняет и огромное число органических соединений, и зависимость свойств этих соединений от их химического строения. Она же полностью подтверждает основные принципы теории химического строения, разработанные выдающимся русским ученым А. М. Бутлеровым.
Основные положения этой теории (иногда ее называют структурной):
1) атомы в молекулах соединены между собой в определенном порядке химическими связями согласно их валентности;
2) свойства вещества определяются не только качественным составом, но и строением, и взаимным влиянием атомов.
3) по свойствам вещества можно определить его строение, а по строению – свойства.
Важным следствием теории строения был вывод о том, что каждое органическое соединение должно иметь одну химическую формулу, отражающую ее строение. Такой вывод теоретически обосновывал хорошо известное уже тогда явление изомерии,— существование веществ с одинаковым молекулярным составом, но обладающих различными свойствами.
Изомеры – вещества, одинаковые по составу, но разные по строению
Структурные формулы. Существование изомеров потребовало использования не только простых молекулярных формул, но и структурных формул, отражающих порядок связи атомов в молекуле каждого изомера. В структурных формулах ковалентная связь обозначается черточкой. Каждая черточка означает общую электронную пару, связывающую атомы в молекуле.
Структурная формула — условное изображение строения вещества с учетом химических связей.
Классификация органических соединений.
Для классификации органических соединений по типам и построения их названий в молекуле органического соединения принято выделять углеродный скелет и функциональные группы.
Углеродный скелет представляет собой последовательность химически связанных между собой атомов углерода.
Типы углеродных скелетов. Углеродные скелеты разделяют на ациклические (не содержащие циклов), циклические и гетероциклические.
В гетероциклическом скелете в углеродный цикл включается одни или несколько атомов, отличных от углерода. В самих углеродных скелетах нужно классифицировать отдельные атомы углерода по числу химически связанных с ними атомов углерода. Если данный атом углерода связан с одним атомом углерода, то его называют первичным, с двумя — вторичным, тремя — третичным и четырьмя — четвертичным.
Углеводороды – соединения, в которых атомы углерода связаны только с атомами водорода.
Углеводороды признаны в органической химии родоначальными. Разнообразные соединения рассматриваются как производные углеводородов, полученные введением в них функциональных групп.
Функциональные группы. В большинстве органических соединений, кроме атомов углерода и водорода, содержатся атомы других элементов (не входящие в скелет). Эти атомы или их группировки, во многом определяющие химические и физические свойства органических соединений, называют функциональными группами.
Функциональная группа оказывается окончательным признаком, по которому соединения относятся к тому или иному классу.
Важнейшие функциональные группы
Гомологический ряд. Для описания органических соединений полезным является понятие гомологического ряда. Гомологический ряд образуют соединения, отличающиеся друг от друга на группу —СН2— и обладающие сходными химическими свойствами. Группы СН2 называются гомологической разностью.
Состав молекул всех членов гомологического ряда может быть выражен одной общей формулой. Для рассмотренного гомологического ряда предельных углеводородов такой формулой будет СnН2n+2, где n — число атомов углерода.
Номенклатура органических соединений. В настоящее время признана систематическая номенклатура ИЮПАК (IUРАС — Международный союз теоретической и прикладной химии).
По правилам ИЮПАК название органического соединения строится из названия главной цепи, образующего корень слова, и названий функций, используемых в качестве приставок или суффиксов.
Для правильного построения названия необходимо провести выбор главной цепи и нумерацию атомов углерода в ней.
Нумерацию атомов углерода в главной цепи начинают с того конца цепи, ближе к которому расположена старшая группа. Если таких возможностей оказывается несколько, то нумерацию проводят таким образом, чтобы либо кратная связь, либо другой заместитель, имеющийся в молекуле, получили наименьший номер.
В карбоциклических соединениях нумерацию начинают от того атома углерода, при котором находится старшая характеристическая группа. Если при этом невозможно выбрать однозначную нумерацию, то цикл нумеруют так, чтобы заместители имели наименьшие номера.
В группе циклических углеводородов особо выделяются ароматические углеводороды, для которых характерно наличие в молекуле бензольного кольца. Некоторые широко известные представители ароматических углеводородов и их производных имеют тривиальные названия, использование которых разрешено правилами ИЮПАК: бензол, толуол, фенол, бензойная кислота.
Радикал С6Н5—, образованный из бензола, называется фенил, а не бензил. Бензилом называют радикал С6Н5СН2—, образованный из толуола.
Далее в суффикс выносится название самой старшей характеристической группы в молекуле с указанием ее положения цифрой. Прочие заместители обозначаются с помощью приставок. При этом они перечисляются не в порядке старшинства, а по алфавиту. Положение заместителя указывается цифрой перед приставкой, например: 3-метил; 2-хлор и т. п. Если в молекуле имеется несколько одинаковых заместителей, то перед названием соответствующей группы словом указывается их количество (например, диметил-, трихлор- и т. д.). Все цифры в названиях молекул отделяются от слов дефисом, а друг от друга запятыми. Углеводородные радикалы имеют свои названия.
Предельные углеводородные радикалы:
Непредельные углеводородные радикалы:
Ароматические углеводородные радикалы:
В качестве примера назовем следующее соединение:
1) Выбор цепи однозначен, следовательно, корень слова — пент; далее следует суффикс −ен, указывающий на наличие кратной связи;
2) порядок нумерации обеспечивает старшей группе (—ОН) наименьший номер;
Следовательно, приведенное соединение называется пентен-4-ол-2.
Тривиальная номенклатура представляет собой совокупность несистематических исторически сложившихся названий органических соединений (пример: ацетон, уксусная кислота, формальдегид и т. д.).
Выше было показано, что способность атомов углерода к образованию четырех ковалентных связей, в том числе и с другими атомами углерода, открывает возможность существования нескольких соединений одного элементного состава — изомеров. Все изомеры делят на два больших класса — структурные изомеры и пространственные изомеры.
Структурными называют изомеры с разным порядком соединения атомов.
Пространственные изомеры имеют одинаковые заместители у каждого атома углерода и отличаются лишь их взаимным расположением в пространстве.
Структурные изомеры. В соответствии с приведенной выше классификацией органических соединений по типам среди структурных изомеров выделяют три группы:
1 ) соединения, отличающиеся углеродными скелетами:
2) соединения, отличающиеся положением заместителя или кратной связи в молекуле:
3) соединения, содержащие различные функциональные группы и относящиеся к различным классам органических соединений:
Пространственные изомеры (стереоизомеры). Стереоизомеры можно разделить на два типа: геометрические изомеры и оптические изомеры.
Геометрическая изомерия характерна для соединений, содержащих двойную связь или цикл. В таких молекулах часто возможно провести условную плоскость таким образом, что заместители у различных атомов углерода могут оказаться по одну сторону (цис-) или по разные стороны (транс-) от этой плоскости. Если изменение ориентации этих заместителей относительно плоскости возможно только за счет разрыва одной из химических связей, то говорят о наличии геометрических изомеров. Геометрические изомеры отличаются своими физическими и химическими свойствами.
Взаимное влияние атомов в молекуле.
Все составляющие молекулу атомы находятся во взаимосвязи и испытывают взаимное влияние. Это влияние передается в основном через систему ковалентных связей с помощью так называемых электронных эффектов.
Электронными эффектами называют смещение электронной плотности в молекуле под влиянием заместителей.
В зависимости от того, удаляется ли электронная плотность от рассматриваемого атома углерода или приближается к нему, индуктивный эффект называют отрицательным (-I) илиположительным (+I). Знак и величина индуктивного эффекта определяются различиями в электроотрицательности между рассматриваемым атомом углерода и группой, его вызывающей.
Электронодонорные заместители, т. е. атом или группа атомов, смещающие электронную плотность к атому углерода, проявляют положительный индуктивный эффект(+I-эффект).
+I-эффект проявляют алифатические углеводородные радикалы, т. е. алкильные радикалы (метил, этил и т. д.).
Индуктивный эффект проявляется и в случае, когда связанные атомы углерода различны по состоянию гибридизации. Так, в молекуле пропена метильная группа проявляет +I-эффект, поскольку атом углерода в ней находится в sp3-гибридном состоянии, а sp2-гибридизованный атом (при двойной связи) выступает в роли электроноакцептора, так как имеет более высокую электроотрицательность :
Наличие электронных эффектов ведет к перераспределению электронной плотности в молекуле и появлению частичных зарядов на отдельных атомах. Это определяет реакционную способность молекулы.
Классификация органических реакций
− Классификация по типу разрыва химических связей в реагирующих частицах. Из их числа можно выделить две большие группы реакций — радикальные и ионные.
Радикальные реакции — это процессы, идущие с гомолитическим разрывом ковалентной связи. При гомолитическом разрыве пара электронов, образующая связь, делится таким образом, что каждая из образующихся частиц получает по одному электрону. В результате гомолитического разрыва образуются свободные радикалы:
Нейтральный атом или частица с неспаренным электроном называется свободным радикалом.
Ионные реакции — это процессы, идущие с гетеролитическим разрывом ковалентных связей, когда оба электрона связи остаются с одной из ранее связанных частиц:
В результате гетеролитического разрыва связи получаются заряженные частицы: нуклеофильная и электрофильная.
Нуклеофильная частица (нуклеофил) — это частица, имеющая пару электронов на внешнем электронном уровне. За счет пары электронов нуклеофил способен образовывать новую ковалентную связь.
−Классификация по составу и строению исходных веществ и продуктов реакции. В органической химии все структурные изменения рассматриваются относительно атома (или атомов) углерода, участвующего в реакции. Наиболее часто встречаются следующие типы превращений:
В соответствии с вышеизложенным хлорирование метана под действием света классифицируют как радикальное замещение, присоединение галогенов к алкенам — как электрофильное присоединение, а гидролиз алкилгалогенидов — как нуклеофильное замещение.






























