Что называется суспензией эмульсией и истинным раствором
Что представляют собой суспензия и эмульсии в химии? Как их описывают?
Содержание:
На нашей планете многие вещества существуют в виде дисперсных систем. Дисперсные системы – это гетерогенная система, которая состоит из двух и более фаз. Одна фаза должна быть мелко раздроблена и равномерно распределена в другой сплошной фазе.
Характеристика дисперсных систем
Дисперсные системы состоят из двух систем:
Дисперсионная среда и дисперсная фаза могут существовать в различных агрегатных состояниях.
Дисперсная фаза
Дисперсионная среда
Примеры
Лекарственные препараты часто представлены в виде суспензий и эмульсий, которые также являются дисперсными системами. В суспензиях в качестве дисперсионной среды выступает жидкость, а дисперсной фазы – твердые частицы. Эмульсии – это жидкая среда, в которой равномерно распределены жидкие капли другой фазы.
Что такое суспензии в химии
Суспензии обладают агрегативной неустойчивостью, т. е. низкой способностью противостоять укрупнению частиц фазы. Частицы в суспензиях, несмотря на свою мизерность, достаточно крупны, чтобы оказывать противостояние броуновскому движению. Они сравнительно быстро всплывают или выпадают в осадок. Суспензии достаточно неустойчивы.
Примеры суспензий в химии:
Что такое эмульсии в химии
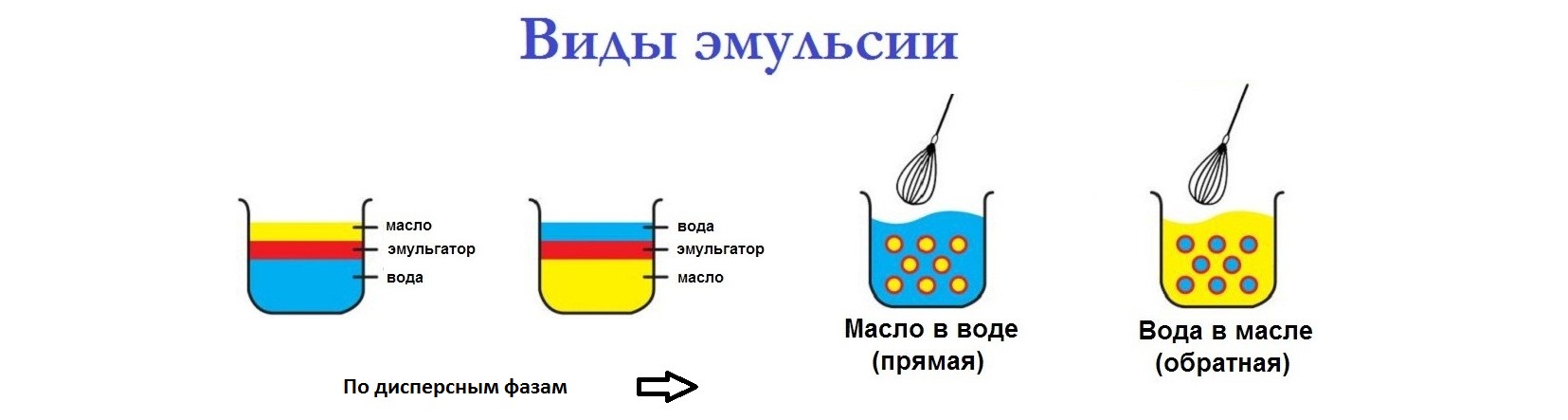
Эмульсии бывают прямыми и обратными. Прямые эмульсии образуются в том случае, если в полярной среде распределяются капли неполярной жидкости (масло в воде). Обратные эмульсии формируются при распределении в неполярной среде полярных частиц вещества (вода в масле). Эмульсии обладают небольшой устойчивостью.
Примеры эмульсий в химии:
Эмульсии и суспензии
К жидким лекарственным формам относятся растворы, слизи, эмульсии, суспензии, настои и отвары, настойки, жидкие экстракты, микстуры. В рамках данной статьи будет произведен обзор суспензии и эмульсий + разницы между ними. Такое большое разнообразие жидких форм создает некие сложности в классификации и понимании.
Что такое суспензия
Суспензии (взвеси) – жидкие лекарственные формы, в которых твердые мелкораздробленные нерастворимые лекарственные вещества находятся во взвешенном состоянии в какой-либо жидкости.
Согласно Государственной Фармакопее
Суспензии – жидкая лекарственная форма, представляющая собой гетерогенную дисперсную систему, содержащую одно или несколько твердых действующих веществ, распределенных в жидкой дисперсионной среде.
Суспензии представляют собой дисперсные системы, состоящие из дисперсионной среды (вода, растительное масло, глицерин и т.п.) и дисперсной фазы (частицы твердых лекарственных веществ, практически нерастворимые в данной жидкости). Назначают суспензии для наружного и внутреннего употребления. Некоторые суспензии применяют парентерально. При этом надо иметь в виду, что суспензии следует вводить внутримышечно или в полости тела.
Чем меньше размер дисперсной фазы в суспензии, тем более (при прочих равных условиях) выражено ее терапевтическое действие. У суспензий, как и у других лекарственных форм, имеются свои преимуществ и недостатки. Они оказывают пролонгированное действие на организм. При назначении суспензий снижается отрицательное воздействие желудочного сока на лекарственные вещества, находящиеся в виде мелких частиц.
Преимущества суспензий
Недостатком суспензий является возможность гидролитического разложения лекарственного вещества при длительном взаимодействии с дисперсионной (в основном водной) средой, что проявляется в процессе их хранения.
Пример суспензий
Особенности суспензий
Одной из важнейших особенностей суспензий является их седиментационная (кинетическая) и агрегативная неустойчивость, которая определяет способы изготовления, хранения и приема данной лекарственной формы. Для обеспечения высокой эффективности препарата суспензии должны обладать высокой агрегативной устойчивостью — способностью противостоять укрупнению частиц и образованию агломератов, кинетической устойчивостью — способностью противостоять оседанию частиц и сохранять равномерное распределение частиц по всему объему суспензии, а также иметь низкую скорость седиментации.
Обычно частицы дисперсной фазы настолько велики (более 10 мкм), что оседают под действием силы тяжести (седиментируют). Суспензии, в которых седиментация идёт очень медленно из-за малой разницы в плотности дисперсной фазы и дисперсионной среды, иногда называют взвесями.
Что такое Эмульсия
Эмульсия – это жидкая лекарственная форма, в которой нерастворимые в воде жидкости (жирные масла, бальзамы) находятся в водной среде во взвешенном состоянии в виде мельчайших капель. Внешне эмульсии имеют сходство с молоком.
Согласно Государственной Фармакопее
Эмульсии – жидкие лекарственные формы, представляющие собой гетерогенную двухфазную дисперсную систему с жидкой дисперсной фазой и жидкой дисперсионной средой
Самое главное отличие эмульсий от суспензий и других лекарственных форм заключается в том, что Эмульсии могут быть типа масло/вода и вода/масло. Эмульсии могут расслаиваться, но при взбалтывании должны легко восстанавливаться. Для обеспечения устойчивости в состав эмульсий вводят эмульгаторы.
По способу приготовления эмульсии подразделяют на масляные (Emulsa oleosa) и семенные (Emulsa seminalia).
Масляные эмульсии готовят из жидких масел: касторового (Oleum Ricini), миндального (Oleum Amygdalarum), рыбьего жира (Oleum jecoris) и др.
Чтобы из масла и воды образовалась эмульсия, необходимо эмульгировать масло, т.е. разделить его на мельчайшие капли. С этой целью масло смешивают со специальными веществами – эмульгаторами. В качестве эмульгаторов используют камеди, например камедь абрикосовую (Gummi Armeniacae), а также желатозу (Gelatosa).
Примеры эмульсий
Чаще всего эмульсии встречаются в лекарствах для наружного применения: бепантнен, фенистил, локойд и др; они равномерно наносятся на кожу, быстро всасываются, высыхают, не оставляют жирного блеска и не пачкают одежду.
Разница между эмульсиями и суспензиями
В этом разделе мы рассмотрим разницу между эмульсиям и суспензиями. Сказать правде в глаза, в случае эмульсий и суспензий тяжело заметить один и тот же препарат в разных лекарственных формах, поэтому сравнительный анализ затруднен и дальнейшее сравнение будет строиться на объективных факторах и свойствах этих лекарственных форм:
Суспензии
Эмульсии
Примеры суспензий и эмульсий
Далее будут перечислены примеры лекарств суспензий и лекарств эмульсий:
Химия. 11 класс
Конспект урока
Урок № 6. Дисперсные системы
Перечень вопросов, рассматриваемых в теме: урок посвящён изучению истинных растворов и дисперсных систем: способам выражения концентрации растворов, видам дисперсных систем, их свойствам, способам коагуляции золей, строению гелей.
Гель – полутвёрдая трёхмерная ячеистая структура, каркас которой образован коллоидными частицами, а в прослойках между частицами удерживается дисперсионная среда.
Дисперсионная среда – сплошная фаза, составная часть дисперсной системы, в которой равномерно распределены частицы дисперсной фазы.
Дисперсная система – гетерогенная система, состоящая, как минимум, из двух фаз, одна из которых мелко раздроблена и равномерно распределена в другой, сплошной фазе.
Дисперсная фаза – мелко раздробленные частицы, равномерно распределённые в дисперсионной среде.
Гетерогенная система – неоднородная система, в которой компоненты находятся в разных фазах и между ними существует видимая граница раздела фаз.
Гомогенная система – однородная система, все компоненты которой находятся в одной фазе, граница раздела фаз между компонентами отсутствует.
Истинный раствор – гомогенная система, состоящая из двух или более компонентов, состав которой в определённых пределах можно изменять без нарушения однородности.
Коагуляция – процесс слипания коллоидных частиц в более крупные агрегаты.
Опалесценция – изменение окраски бесцветного коллоидного раствора с желтоватой в проходящем свете на голубую в отраженном свете.
Седиментация – процесс оседания крупных частиц дисперсной фазы.
Фаза – часть системы, однородная по составу и свойствам, отделённая от окружающей среды видимой границей раздела.
Электрофорез – движение коллоидных частиц золя в постоянном электрическом поле к одному из электродов.
Эмульсия – грубодисперсная система, в которой одна жидкая фаза в виде отдельных мелких капель равномерно распределена в другой жидкости, при этом жидкости взаимно нерастворимы.
Эффект Тиндаля – образование светлого конуса в отраженном свете при прохождении через дисперсную систему луча света.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Истинным раствором называется гомогенная система, состоящая из нескольких компонентов, состав которой в определённых пределах можно менять без нарушения однородности.
Растворимостью называется такое количество вещества, которое можно при данной температуре растворить в 100 г растворителя. Абсолютно нерастворимых веществ в природе не существует.
Молярная концентрация показывает количество растворённого вещества в 1 литре раствора. Сокращенно молярная концентрация, или молярность, обозначается буквой М, например, 1 М – один моль на литр. 
Для того, чтобы найти молярную концентрацию по величине известной массовой доли, необходимо знать плотность раствора. При этом массовая доля должна быть выражена не в процентах, а в долях, а плотность – в г/л.

С истинными растворами мы постоянно встречаемся в жизни. Пьём чай с сахаром, консервируем овощи. В сельском хозяйстве используют растворы минеральных удобрений и средств для борьбы с вредителями и болезнями растений. Растворы используют в промышленности, в медицине, в учебных и научно-исследовательских химических лабораториях.
Дисперсной называется гетерогенная система, состоящая, как минимум, из двух фаз, одна из которых мелко раздроблена и равномерно распределена во второй, сплошной фазе. В отличие от истинных растворов, дисперсная система неоднородна, а между составляющими её фазами всегда существует граница раздела. Мелкораздробленная фаза называется дисперсной фазой, а сплошная фаза – дисперсионной средой. В зависимости от размера частиц дисперсной фазы различают грубодисперсные (размер частиц больше 100 нм) и тонкодисперсные (от 1 до 100 нм), или коллоидные системы. Если размер частиц дисперсной фазы становится меньше 1 нм, система перестает быть гетерогенной, образуется истинный раствор. В истинном растворе вещество раздроблено до отдельных молекул или ионов. В зависимости от агрегатного состояния дисперсной фазы и дисперсионной среды дисперсные системы разделяют на суспензии, эмульсии, пены и аэрозоли. В суспензии твёрдые частицы распределены в жидкости. Эмульсия состоит из мелких капель жидкости, равномерно распределённых в другой жидкости, причем эти жидкости взаимно нерастворимы. Пена – это мелкие пузырьки газа в жидкости. Аэрозоль представляет собой газообразную среду, в которой распылены мелкие твёрдые или жидкие частицы.
Получение и свойства коллоидных растворов
Тонкодисперсные коллоидные системы получили название «золь». Золи могут быть образованы как неорганическими веществами, так и органическими макромолекулами, размеры которых превышают 1 нм, например, белками. Приготовить золь можно смешиванием малорастворимого вещества с растворителем (раствор крахмала, яичного белка), так и с помощью химических реакций ионного обмена, гидролиза, окисления-восстановления, в которых один из продуктов реакции не растворяется в жидкости.
Если в U-образную стеклянную трубку налить золь гидроксида железа и погрузить в каждое колено трубки графитовые электроды, подсоединив их к источнику постоянного электрического тока, то жидкость в одном колене станет светлее, в другом интенсивность окраски увеличится. Происходит это, так как коллоидные частицы движутся в постоянном электрическом поле к одному из электродов. Это явление получило название «электрофорез».
Образование заряда на поверхности коллоидных частиц
Для золей, как и для истинных растворов, характерно броуновское движение, а тяжёлые и крупные частицы грубодисперсных систем в броуновском движении не участвуют. Одноимённые заряды коллоидных частиц препятствуют их слипанию, поэтому золи длительное время остаются устойчивыми. Размеры частиц дисперсной фазы в грубодисперсных системах слишком большие, со временем они оседают – происходит седиментация.
Коагуляция коллоидных растворов
Если к золю добавить раствор электролита, произойдет нейтрализация заряда коллоидных частиц. Золь потеряет устойчивость, частицы начнут слипаться. Слипание коллоидных частиц называется коагуляцией. Коагуляцию можно вызвать длительным нагреванием золя, а также сливанием золей с противоположно заряженными частицами. Если коллоидные частицы слабо взаимодействуют с дисперсионной средой, то в результате коагуляции образуется осадок. Если коллоидные частицы хорошо взаимодействуют с растворителем, то они захватывают часть жидкости, в результате образуется гель. Гель – трёхмерная ячеистая структура, каркас которой образован коллоидными частицами, а в ячейках удерживается жидкость.
Дисперсные системы в природе и на службе у человека
Коллоидные растворы широко распространены в природе. Плазма крови, яичный белок, сырая нефть, речная и озёрная вода, почвенный раствор являются золями. Дисперсными системами являются облака, туман, дым, морская пена, молоко, газированная вода. В промышленности и быту человек использует эмульсионные краски, клеи, лаки, косметические и лечебные гели и шампуни. В пищевой промышленности дисперсными системами являются тесто, желе, студни, соусы, бульоны, мармелад, суфле. Без преувеличения можно сказать, что коллоидная химия – это химия реальных систем.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Приготовление насыщенного раствора
Условие задачи: Для приготовления насыщенного раствора поваренной соли надо в 100 г воды растворить 36 г хлорида натрия. Какое количество (моль) поваренной соли будет растворено в 360 г насыщенного раствора? Ответ запишите с точностью до десятых долей.
Шаг первый: найдём массу насыщенного раствора соли, в котором растворено 36 г хлорида натрия. Для этого сложим массу растворителя и растворённого вещества:
Шаг второй: найдём массу хлорида натрия, которая содержится в 360 г насыщенного раствора. Для этого составим пропорцию:
В 136 г насыщенного раствора содержится 36 г хлорида натрия;
в 360 г такого же раствора содержится т г хлорида натрия.
т = (360·36) : 136 = 95,3 (г).
Шаг третий: вычислим молярную массу хлорида натрия:
М = 23 + 35 = 58 (г/моль).
Шаг четвертый: найдём, сколько моль хлорида натрия содержится в 95,3 г.
Для этого массу хлорида натрия разделим на его молярную массу:
2. Расчёт объёма раствора, который можно приготовить из раствора известной концентрации
Шаг первый: найдём массу 200 мл 12%-ного раствора.
Для этого умножим объём раствора на его плотность:
Шаг второй: найдём массу гидроксида натрия, которая содержится в 226 г 12%-ного раствора.
Для этого составим пропорцию:
В 100 г раствора содержится 12 г гидроксида натрия;
в 226 г раствора содержится т г гидроксида натрия.
т = (226·12) : 100 = 27,12 (г)
Шаг третий: найдём количество моль гидроксида натрия, которое содержится в 27,12 г.
Для этого вычислим молярную массу гидроксида натрия:
М = 23 + 16 + 1 = 40 (г/моль).
Теперь разделим массу гидроксида натрия на его молярную массу:
27,12 : 40 = 0,68 (моль).
Шаг четвёртый: Найдём объём раствора, в котором это количество гидроксида натрия составит концентрацию 0,5 М.
Для этого составим пропорцию:
в 1000 мл раствора содержится 0,5 моль гидроксида натрия;
в V мл раствора содержится 0,68 моль гидроксида натрия.
ГК «Униконс»
Продвижение и реализация комплексных пищевых добавок, антисептиков и др. продукции.
«Антисептики Септоцил»
Септоцил. Бытовая химия, антисептики.
«Петритест»
Микробиологические экспресс-тесты. Первые результаты уже через 4 часа.
«АльтерСтарт»
Закваски, стартовые культуры. Изготовление любых заквасок для любых целей.
5.4. ДИСПЕРСНЫЕ И КОЛЛОИДНЫЕ СИСТЕМЫ
Важная роль в пищевой технологии принадлежит дисперсным и коллоидным системам и их свойствам.
Дисперсные системы гетерогенны и состоят из двух фаз. Одна из них — сплошная, называется дисперсионной средой. Другая — раздробленная и распределенная в первой, называется дисперсной фазой.
Дисперсными системами являются большинство продуктов питания, сырье и полуфабрикаты: хлеб, мука, шоколад, сыры, творог, сухое молоко, соки, шампанское, пиво, конфеты и т. п.
5.4.1. Классификация дисперсных систем
Все дисперсные системы классифицируют по степени дисперсности.
Дисперсные системы с частицами, размер которых превышает 10
3 см, относятся к грубодисперсным системам. Эти частицы при распределении в жидкости или газе, где они постепенно оседают или всплывают, наблюдаются визуально.
Дисперсные системы классифицируются не только по размерам частиц, но и по агрегатному состоянию дисперсной фазы и дисперсионнойсреды.
Сочетание трех агрегатных состояний (твердое, жидкое и газообразное) дает 9 типов дисперсных систем (см. табл. 3). Условно их обозначают дробью, числитель которой указывает на агрегатное состояние дисперсной фазы, а знаменатель— дисперсионной среды. Например, обозначение Г/Ж показывает, что система состоит из газообразной дисперсной фазы и жидкой дисперсионной среды (газообразное вещество в жидкости).
Типы дисперсных систем
5.4.2. Коллоидные системы
Дисперсные системы с частицами коллоидных размеров принято называть золями (от лат. solutio — раствор).
Системы с газовой дисперсионной средой независимо от природы газа называют аэрозолями. Системы с жидкой дисперсионной средой — лиозолями (от греч. lios — жидкость).
По размеру частиц золи занимают промежуточное положение между истинными растворами и грубодисперсными системами — порошками, суспензиями и эмульсиями.
Коллоидные системы образуются двумя путями.
При этом необходимыми условиями образования коллоидных систем являются нерастворимость вещества дисперсной фазы в дисперсионной среде; достижение частицами дисперсной фазы коллоидной дисперсности; наличие стабилизатора, сообщающего коллоидной системе агрегативную устойчивость.
Стабилизаторами могут быть вещества, специально вводимые в дисперсионную среду, например, поверхностно-активные вещества или продукты взаимодействия дисперсной фазы с дисперсионной средой. Стабилизаторы создают вокруг коллоидных частиц адсорбционный защитный слой, препятствующий их агрегатированию.
В производстве различных пищевых продуктов диспергирование и конденсация занимают одно из ведущих мест. Это обусловлено особенностями вещества в дисперсном состоянии, которые обеспечивают удобства фасования, транспортирования, дозирования, способствуют увеличению скоростей химических и биохимических реакций и процессов растворения, сорбции, экстракции и других процессов.
Диспергирование используют при дроблении и измельчении зерна в муку, какао-бобов в какао тертое и какао-порошок, сахара в сахарную пудру, в консервной промышленности при гомогенизации плодово-ягодных пюре и т. п.
Конденсация возникает в ректификационных аппаратах при получении спирта, кристаллизации сахара, выпаривании растворов, оклейке вин и т. д.
Коллоидные системы обладают молекулярно-кинетическими свойствами, обусловленными самопроизвольным движением частиц. Это такие свойства, как диффузия, осмотическое давление и распределение частиц по высоте.
На коллоидные частицы, распределенные в дисперсионной среде, действуют две противоположно направленные силы: сила тяжести и сила диффузии. Под действием силы тяжести частицы стремятся осесть на дно — седиментировать (от латинского слова sedimentum — осадок). Силы диффузии же стремятся распределить частицы равномерно по всему объему системы. Таким образом, дисперсные системы способны сохранять определенное распределение частиц по объему. Эта способность называется седиментационной или кинетической устойчивостью.
Грубодисперсные системы кинетически неустойчивы, их частицы велики и поэтому под действием силы тяжести оседают на дно. Молекулярные системы (газы, растворы) обладают очень высокой кинетической устойчивостью. Кинетическая устойчивость коллоидных систем зависит от размеров их частиц: чем меньше размер частиц, тем более кинетически устойчива коллоидная система.
5.4.3. Микрогетерогенные системы
СУСПЕНЗИИ
Суспензии представляют собой дисперсные системы с твердой дисперсной фазой и жидкой дисперсионной средой. К ним относятся фруктовые и овощные пасты, помадные конфетные массы, какао тертое и др.
ЭМУЛЬСИИ
Дисперсные системы, состоящие из жидкой дисперсной фазы и жидкой дисперсионной среды, называются эмульсиями. Обязательное условие образования эмульсии — нерастворимость вещества дисперсной фазы в дисперсионной среде.
Обычно эмульсии получают методом механического диспергирования. Для этого используют различные мешалки, смесители, гомогенизаторы, коллоидные мельницы и ультразвук.
Жидкости, из которых получают эмульсии, нерастворимы друг в друге и, следовательно, отличаются по своим свойствам. Практически одной из жидкостей всегда является вода, а другой — какая-либо неполярная, нерастворимая в воде жидкость, например, масло.
Эмульсии — неустойчивые системы. Неустойчивость этой системы проявляется в самопроизвольном слиянии капелек дисперсной фазы — коалесценции, что приводит к разрушению эмульсии и разделению ее на два слоя.
Устойчивость эмульсиям может придать только третий компонент — стабилизатор или эмульгатор. Роль эмульгатора в образовании устойчивой эмульсии заключается, во-первых, в том, что он адсорбируется на границе раздела фаз масло — вода (М/В) и снижает межфазное поверхностное натяжение, т. е. является поверхностно- активным веществом, а во-вторых, концентрируясь на поверхности капелек дисперсной фазы, эмульгатор образует механически прочный слой (пленку). Наличие такой защитной пленки на поверхности частиц дисперсной фазы препятствуют их слиянию, т. е. предохраняет эмульсию от коалесценции.
Природа эмульгатора определяет не только устойчивость, но и тип эмульсии. Эмульгаторы, растворимые в воде, способствуют образованию прямых эмульсий (М/В); эмульгаторы, растворимые в неполярных жидкостях, дают обратные эмульсии (В/М).
К представителям эмульсий относится ряд важнейших жиросодержащих продуктов, например, молоко, сливки, сливочное масло, сметана и майонез. Все это — эмульсии.
АЭРОЗОЛИ И ПОРОШКИ
Аэрозоли и порошки — это дисперсные системы, дисперсионной средой которых является газ (воздух), а дисперсной фазой могут быть твердые частицы или капельки жидкости.
Аэрозоли имеют большое практическое значение в ряде отраслей пищевой промышленности. К типичным аэрозолям относятся водяной туман, топочный дым, мучная и сахарная пыль. В ряде случаев в промышленности прибегают к искусственному получению аэрозолей. Так, для высушивания соки, пюре, молоко распыляют до мельчайших капелек в сухом горячем воздухе. Из образующегося аэрозоля благодаря его большой удельной поверхности испарение влаги идет очень интенсивно, и сушка заканчивается за 15-20 с.
Образование аэрозолей может привести к нежелательным и опасным последствиям. Так, пыль многих веществ — муки, сахара, крахмала, угля — образует с воздухом взрывоопасные смеси.
Порошки можно рассматривать как осажденные аэрозоли с твердыми частицами. Однако частицы в них могут быть более крупными и достигать в диаметре 1-2 мм. Размер частиц промышленных порошков определяется их целевым назначением и часто является одним из основных показателей качества продукта. Например, дисперсность и распределение частиц по размерам в какао-порошке влияют на вкусовые качества и пищевую ценность этого продукта. Степень помола зерна оказывает влияние на качество муки.
ПЕНЫ
Высококонцентрированные дисперсные системы, в которых дисперсионная среда — жидкость, а дисперсная фаза — газ, называются пенами.
Пузырьки газа в пенах имеют большие размеры, форму многогранников и отделены друг от друга очень тонкими слоями дисперсионной среды.
Для получения пен применяют диспергационные методы: интенсивное встряхивание или перемешивание жидкости.
Устойчивую пену можно получить только в присутствии стабилизатора — пенообразователя. Это связано с тем, что поверхность жидкости, соприкасающаяся с газообразной средой, находится в особых условиях по сравнению с основной массой жидкости. Эти условия возникают потому, что молекулы поверхностного слоя жидкости в отличие от молекул, находящихся в глубине, подвергаются неодинаковому притяжению молекул жидкости и газа. Каждая молекула внутри жидкости со всех сторон притягивается соседними молекулами, расположенными на расстоянии радиуса сферы действия межмолекулярных сил. В результате силы притяжения компенсируются, и равнодействующая этих сил равна нулю. У молекул поверхностного слоя часть сферы действия межмолекулярных сил находится в газовой фазе, плотность которой меньше плотности жидкости, поэтому равнодействующая всех сил притяжения будет направлена внутрь жидкости перпендикулярно к ее поверхности. Вследствие этого поверхностные молекулы жидкости всегда находятся под действием силы, стремящейся втянуть их внутрь. Это приводит к тому, что поверхность жидкости всегда стремится сократиться. Этим объясняются и шарообразная форма капли жидкости (шар имеет минимальную поверхность), и идеально гладкая поверхность жидкости в широком сосуде. При увеличении поверхности некоторое число молекул из глубины жидкости переходит на поверхность. Процесс переноса молекул из равновесного состояния в особое состояние молекул поверхностного слоя требует затраты внешней работы. Работа по увеличению площади поверхности жидкости переходит в потенциальную энергию молекул поверхностного слоя— поверхностную энергию. Последняя, в свою очередь, отнесенная к единице поверхности, называется поверхностным натяжением.
Пенообразующие вещества с длинной молекулярной цепью уменьшают поверхностное натяжение, облегчают образование пены и придают ей стабильность, так как они адсорбируются на границе вода-воздух и образуют высоковязкую структурированную пленку, препятствующую стеканию жидкости. В этом случае толщина слоя жидкости между пузырьками воздуха уменьшается медленно, и пена может существовать длительное время.
Пенообразование имеет важное практическое значение. В частности, многие продукты, такие как хлеб, ряд кондитерских изделий, имеют структуру пены, что определяет их вкусовые свойства и пищевую ценность.
5.4.4. Молекулярные коллоиды (растворы высокомолекулярных соединений)
Вещества, имеющие молекулярную массу от 10000 до нескольких миллионов, называются высокомолекулярными соединениями (ВМС). Размеры макромолекул этих соединений в вытянутом состоянии могут достигать 1000 нм и более, т. е. они соизмеримы с размерами частиц ультрамикрогетерогенных (коллоидных) дисперсных систем.
Вследствие большой молекулярной массы и гибкости цепей макромолекул ВМС га растворы обладают специфическими свойствами: способностью образовывать волокна и пленки, эластичностью, набухаемостью, структурообразованием.
К важнейшим природным полимерам относятся белки и полисахариды.
По химической структуре белки являются полиамидами, исходными мономерами для их синтеза служат а-аминокислоты.
Полисахариды представляют собой соединения, состоящие из многих сотен и даже тысяч моносахаридных звёньев. К наиболее важным полисахаридам относятся крахмал, целлюлоза, пектин и др.
Растворы ВМС по своим свойствам аналогичны коллоидным системам. Так же, как и у коллоидных растворов, у них сравнительно невелика скорость диффузии, небольшое осмотическое давление, они не проходят через полунепроницаемые мембраны.
В отличие от золей растворы ВМС образуются самопроизвольно и не нуждаются в стабилизаторе.
Растворению ВМС предшествует его набухание.
Набухание — это самопроизвольный процесс поглощения низкомолекулярного растворителя высокомолекулярным веществом, сопровождающийся увеличением массы и объема последнего. Набухание часто является начальным этапом растворения высокомолекулярных веществ.
Существует ограниченное и неограниченное набухание. При ограниченном набухании объем и масса полимера достигают определенных значений, и дальнейший контакт полимера с растворителем не приводит к каким-либо изменениям. Ограниченно набухший полимер называется студнем. У неограниченного набухания отсутствует предел набухания; с течением времени полимер поглощает все большее количество жидкости и набухание переходит в растворение.
Причиной набухания является диффузия молекул низкомолекулярного растворителя в высокомолекулярное вещество. Между макромолекулами полимера обычно имеются небольшие промежутки, размер которых соизмерим с размером молекул растворителя. Благодаря этому молекулы низкомолекулярной жидкости достаточно быстро проникают между макромолекулами, раздвигая молекулярные цепи.
Набухание включает не только простую диффузию, но и сольватацию макромолекул, т. е. взаимодействие молекул растворителя с молекулами полимера.
При взаимодействии высокомолекулярного вещества с полимером сольватируется не вся макромолекула. Если растворитель полярен, то сольватируются полярные группы, если неполярен — то сольватируются неполярные группы. В зависимости от того, каких групп в полимере больше, он будет быстрее набухать в полярном или неполярном растворителе. Обычно набухание — избирательное явление, так как полимер набухает в жидкостях, близких к нему по химическому строению. Так, углеводородные полимеры типа каучук набухают в неполярных жидкостях — бензине, бензоле. Полимеры, в состав молекул которых входят полярные группы, набухают в воде и спиртах.
Чаще всего жидкой дисперсионной средой в пищевых производствах служит вода. При этом следует учитывать, что часть воды находится в свободном состоянии, а часть — в связанном.
В системах, в состав которых входят биополимеры (высокомолекулярные природные соединения — белки, полисахариды), часть воды, прочно связанная с поверхностью этих макромолекул, образует гидратную оболочку. Например, 1 г яичного альбумина связывает 0,25 г воды, образуя гидратный слой толщиной 0,25 нм.
Свободная же вода служит реакционной средой и растворителем веществ. При участии гидролитических ферментов она вступает во множество реакций, в результате которых образуются новые вещества. Таким образом, свободная вода является и активным участником биохимических реакций.
Мука, состоящая главным образом из сухих протеиновых гелей и крахмальных зерен, при замешивании теста (при взаимодействии с водой) проявляет коллоидные свойства.
Крахмал муки, смоченный водой при комнатной температуре, может адсорбционно связать 35-40% влаги. При более высокой температуре и достаточном количестве воды связывание крахмала с водой увеличивается, и при температуре 60°С и избытке воды происходит процесс клейстеризации крахмала, т. е. нарушение структуры крахмальных зерен и образование коллоидного раствора.
Крахмал, смоченный водой в любом соотношении и в любых условиях, не образует связного теста.
Ведущая роль в образовании теста принадлежит белкам пшеничной муки.
Белки способны набухать в холодной воде и удерживать воду в количестве в 2-2,5 раза больше своей массы. При замешивании теста из пшеничной муки белки при достаточном количестве воды легко и сравнительно быстро (через 3-5 мин) образуют тончайшие нити и пленки, связывающие и склеивающие между собой зерна увлажненного крахмала. Благодаря этому пшеничное тесто приобретает упруговязкопластичные свойства, какими не обладает тесто из других злаков.
Крахмал муки состоит из двух основных фракций — амилозы и амилопектина. Амилоза содержится внутри крахмальных зерен, а амилопектин образует их наружную оболочку. Амилоза отличается меньшей величиной частиц и меньшей молекулярной массой (около 80000), а амилопектин — большей величиной частиц и большей молекулярной массой (115000). Это позволяет рассматривать зерно крахмала как осмотическую ячейку, внутри которой находится растворимая низкомолекулярная фракция — амилоза, обусловливающая избыточное осмотическое давление и приток воды внутрь ячейки.
Гидратация муки при разных температурах зависит от поведения белков и крахмала. В температурном интервале 25-40°С гидратация муки происходит преимущественно за счет белков клейковины. Повышение температуры до 60°С приводит к резкому усилению этого процесса в результате значительного увеличения гидратации крахмала при понижении этой способности у белков клейковины.
Таким образом, набухание пшеничной муки при низкой температуре (25-40°С) в основном протекает вследствие осмотического набухания бежов, а при более высокой температуре (60°С) — в результате осмотического связывания воды крахмалом.
В связи с этим схему образования теста можно представить в следующем виде.
Белки, содержание которых в пшеничной муке составляет 10- 20%, при температуре замеса около 30°С поглощают незначительное количество воды путем взаимодействия гидрофильных групп белка с водой, а значительное количество воды диффундирует внутрь белка в результате наличия в нем избыточного осмотического давления.
Крахмал, содержание которого в пшеничной муке достигает 70%, при той же температуре теста поглощает до 30% воды благодаря активности гидрофильных групп. Так как крахмал количественно преобладает в муке, то содержание влаги, связанное крахмалом и белками клейковины, приблизительно одинаково.
При неограниченном оводнении коллоидов муки часть воды находится в свободном состоянии в капиллярах теста. Незначительная часть растворимых белков, а также сахара и неорганические соли находятся в растворе.
Набухшие белки во время замеса плотно соприкасаются друг с другом и образуют сплошную белковую сетку с адсорбционно связанными с ними, слабо набухшими крахмальными зернами. В белковую сетку, кроме того, входят другие нерастворимые вещества. Это приводит к образованию массы (теста), обладающей упруговязкопластичными свойствами.
Недостаточное количество воды при замесе теста приводит к получению несвязной массы увлажненного сырья. При избыточном количестве воды, добавляемой к муке, не образуется связного теста, а получается мучная болтушка, в которой частицы набухшего белка разделены водными оболочками, препятствующими соприкосновению их и образованию клейковинных нитей.
Тесто, используемое для мучных кондитерских изделий, — более сложный комплекс, так как в состав его кроме муки и воды входят и другие виды сырья, в первую очередь сахар и жир, влияющие на набухаемость коллоидов муки.
Сахар, присутствующий в кондитерском тесте в виде водного раствора, оказывает влияние на степень набухания белков клейковины. С увеличением концентрации сахара степень набухания белков снижается.
Жир, адсорбируясь на поверхности белков, образует пленки, препятствующие проникновению воды внутрь макромолекул белков, что ослабляет связь между ними, при этом уменьшается упругость и увеличивается пластичность теста.
Таким образом, регулируя количество сахара и жира, добавляемых при замесе теста, можно получать тесто с определенными физическими свойствами.
5.4.5. Структурообразование в дисперсных системах
Одно из важных свойств дисперсных систем и растворов ВМС — способность их к структурообразованию.
Коллоидные системы, частицы которых удалены друг от друга на достаточно большое расстояние и практически не взаимодействующие между собой, называются свободнодисперсными системами. Такие коллоидные системы по своим свойствам похожи на обычные жидкости. Их вязкость очень мало отличается от вязкости дисперсионной среды.
Дисперсные системы, в которых частицы связаны между собой и не способны к взаимному перемещению, называются связнодис- персными системами. В таких системах частицы дисперсной фазы образуют пространственную сетку или структуру.
Рассмотрим процесс структурообразования на примере пектина при производстве фруктового желе.
Желеобразная консистенция фруктовых консервов достигается благодаря присутствию в сырье пектина, который образует в сахарокислотном растворе пространственную сетку. Пектин при нагревании образует коллоидные растворы. На поверхности молекул пектина адсорбированы молекулы воды, которые создают сольватную (водную) оболочку вокруг частиц пектина. Это препятствует соединению пектиновых молекул для образования пространственной сетки. Для формирования желе необходимо присутствие наряду с пектином Сахаров и кислот.
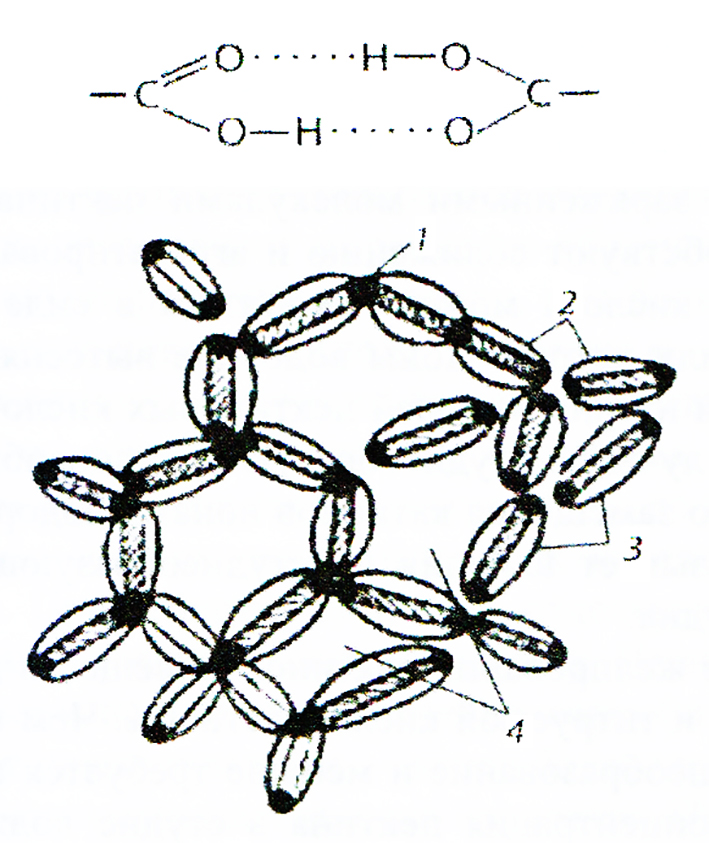
Сила притяжения частиц пектина сосредоточена по краям молекулы. Соединение частиц концами приводит к образованию пространственной сетки, которая охватывает весь объем продукта и служит каркасом студня (см. рис. 25). Укрепление сетки происходит за счет водородных мостиков, которые образуются между карбоксильными и гидроксильными группами соседних пектиновых молекул.
Образовавшиеся ячейки внутри заполнены жидким сахарокислотным раствором. По мере остывания студня тепловое движение замедляется и продолжается процесс укрупнения студня, т. е. сближение молекул и образование цепей. Чем выше концентрация пектина, тем легче сближение молекул и прочнее их сцепление и тем быстрее идет застудневание.
Механическое воздействие на студень при его остывании ослабляет его прочность. Но при нагревании структура студня может быть восстановлена. Это свойство пектиновых студней называется тиксотропией.
Пектино-сахаро-кислотный студень — упруго-эластичная система, в которой каждый компонент выполняет свои функции.
Схема сцепления частиц пектина в желе:
1 — концевые участки, свободные от зарядов; 2 — частицы пектина; 3 — соль- ватные оболочки;
4 — петли пектиновой сетки с дисперсионной средой.
Каркас студня составляет пектин, поэтому прочность студня будет зависеть от вида и качества пектина. Лучше и прочнее студень образуется в присутствии высокометоксилированного пектина, который имеет длинную цепочку с числом метоксильных групп более 70%. Значение имеет также общее содержание пектина в сырье и его природа. Наилучшей желирующей способностью обладает пектин яблок, крыжовника, черной смородины, кожуры цитрусовых. Концентрация пектина должна быть около 1%.
Количество сахара, которое требуется для образования студня, зависит от свойств и количества применяемого пектина. Чем больше пектина и выше его желирующие свойства, тем больше требуется сахара для студнеобразования. Максимальное количество сахара, которое может быть использовано для образования студня, — показатель «сахароемкости» пектина. Он определяет студнеобразующую способность и измеряется в градусах. Это масса сахара, приходящаяся на единицу массы пектина. Для пектина средней студнеобразующей способности содержание сахара должно быть близким к насыщенному раствору при комнатной температуре, т. е. 65%.
Еще один компонент пектинового студня — кислота. Она определяет рН студня. Чем больше диссоциирована кислота, тем более она способствует образованию агрегатов пектиновых молекул, так как при диссоциации кислоты в растворе появляются свободные положительно заряженные ионы водорода (Н + ). Они взаимодействуют с отрицательно заряженными молекулами пектина, нейтрализуют их заряд и способствуют сближению и агрегатированию. Полиметилга-лактуроновая кислота может находиться в виде слаборастворимых солей калия или натрия. Ионы водорода вытесняют и замещают катионы калия и натрия из солей пектиновых кислот, а пектиновые кислоты имеют лучшую студнеобразующую способность, чем их соли. После полного замещения катионов ионами водорода добавление кислоты не оказывает влияния на студнеобразующую способность и прочность студня.
Хорошее желирование пектиновых веществ достигается при рН среды 3,0-3,4 и титруемой кислотности 1%. Чем ниже рН, тем быстрее идет студнеобразование и меньше требуется пектина. Например, при рН 3,1 концентрация пектина в студне должна быть не менее 0,7%, при рН 3,-0,8%, при рН 3,-0,9%. При рН более 3,5 студень образуется непрочный.
Используя способность ВМС к образованию студней, можно получить более сложные дисперсные системы, например, пенообразные кондитерские массы (пастилу). Эти изделия являются в основном агаровым студнем. Он имеет пористую структуру с ячейками микроскопических размеров (до 20 мкм).
В пастильном студне распределены мелкие воздушные пузырьки, и готовая сухая пастила напоминает по своей структуре твердый крем. В производстве пастилы процесс обычного студнеобразования мармелада сочетается с процессом пенообразования (сбивания) яблочно-сахарной смеси.
При сбивании пастилы путем продолжительного встряхивания яблочно-сахарной смеси происходит вспенивание ее, т. е. масса насыщается воздухом; при этом воздух захватывается яблочно-сахарной массой и дробится на мелкие частички. По мере увеличения скорости механического взбалтывания степень раздробленности воздуха увеличивается, размеры пузырьков воздуха уменьшаются, а вязкость массы повышается. Постепенно образуется густая пена, состоящая из мелких пузырьков воздуха, затянутых в тонкую пленку из окружающей полужидкой яблочно-сахарной смеси.
В физико-химическом смысле пена представляет собой двухфазную систему газ-жидкость. В данном случае дисперсной фазой является газ-воздух, а дисперсионной средой — полужидкий раствор сахара, кислоты и пектина. Этот раствор образует оболочку дисперсных частиц газа (воздуха), которая несет на себе поверхностный пограничный слой, отделяющий одну фазу от другой.
В процессе образования пены происходит сильное развитие поверхности раздела на границах газообразной и жидкой фаз. Увеличение поверхности раздела зависит от размеров образующихся воздушных ячеек. Чем меньше размеры последних, тем больше эта поверхность, тем больше сила поверхностного натяжения o.
Сила поверхностного натяжения всегда стремится сократить до минимума общую поверхность раздела всей системы, сделать ее наименьшей. В данном случае она стремится сократить до возможных пределов общую сумму поверхностей отдельных капелек, образующих пенную эмульсию. При действии этой силы отдельные пузырьки воздуха в пене стремятся соединиться в одну массу. Пленка капелек прорывается, отдельные капельки, постепенно сливаясь (агрегируясь) друг с другом, образуют новые пузырьки — капли более крупных размеров, степень дисперсности уменьшается, пена «опадает». Процесс самопроизвольного разрушения пены и эмульсии называется коалесценцией.
В пенах процесс коалесценции идет весьма интенсивно благодаря близкому расположению капелек по отношению друг к другу.
Чтобы сделать пену более устойчивой, стабилизировать ее, в качестве пенообразующего средства (ПАВ) при сбивании пастилы обычно используют белок куриного яйца, который, располагаясь в поверхностном слое пленки пузырьков пены, увеличивает механическую прочность этого слоя и тем самым препятствует прорыванию пленки пузырьков и агрегированию последних.
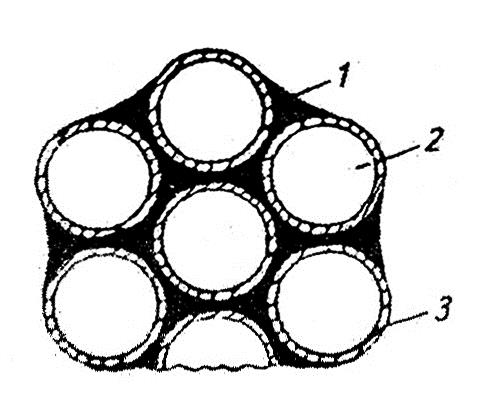
Механизм совмещения студневой и пенной структур при смешивании сбитой массы с агаровой (или мармеладной) можно представить так: при смешивании с холодной сбитой массой горячая масса агарового сиропа или мармелада заполняет воздушные пространства между пузырьками сбитой массы, вытесняя оттуда воздух (см. рис. 26).
При этом прочность пленки структурных элементов массы значительно увеличивается. Последняя возрастает благодаря тому, что температура всей массы поднимается до 50°С и адсорбированный альбуминовый гель пленки при указанной температуре, близкой к свертыванию альбумина, фиксируется в ней в виде плотного коагулята. Одновременно же по мере остывания массы в пространстве между пузырьками происходит формирование прочного агарового (или пектинового) студня. Смешивание сбитой массы с горячей желейной (или мармеладной) массой создает, таким образом, необходимые условия для образования структуры пастилы.
Схема совмещения пенной и студневой структур пастилы:
1 — агаро-сахаро-водный студень; 2 — воздух; 3 — пектино-белково-сахаро- водная пленка.
После остывания массы получается характерный пастельный студень, который отличается от мармеладного только пористой структурой благодаря мельчайшим воздушным включениям, равномерно распределенным в его массе.